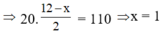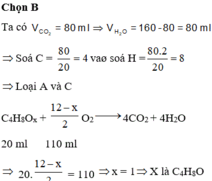Hỗn hợp khí và hơi X gồm C 2 H 4 , C H 3 C H O , C H 3 C O O H . Trộn X với V lít H 2 (đktc) rồi cho qua Ni nung nóng, thu được hỗn hợp Y (gồm khí và hơi). Đốt cháy hoàn toàn Y thu được 0,15 mol C O 2 và 0,2 mol H 2 O . Giá trị của V là
A. 4,48.
B. 2,24.
C. 0,672.
D. 1,12.